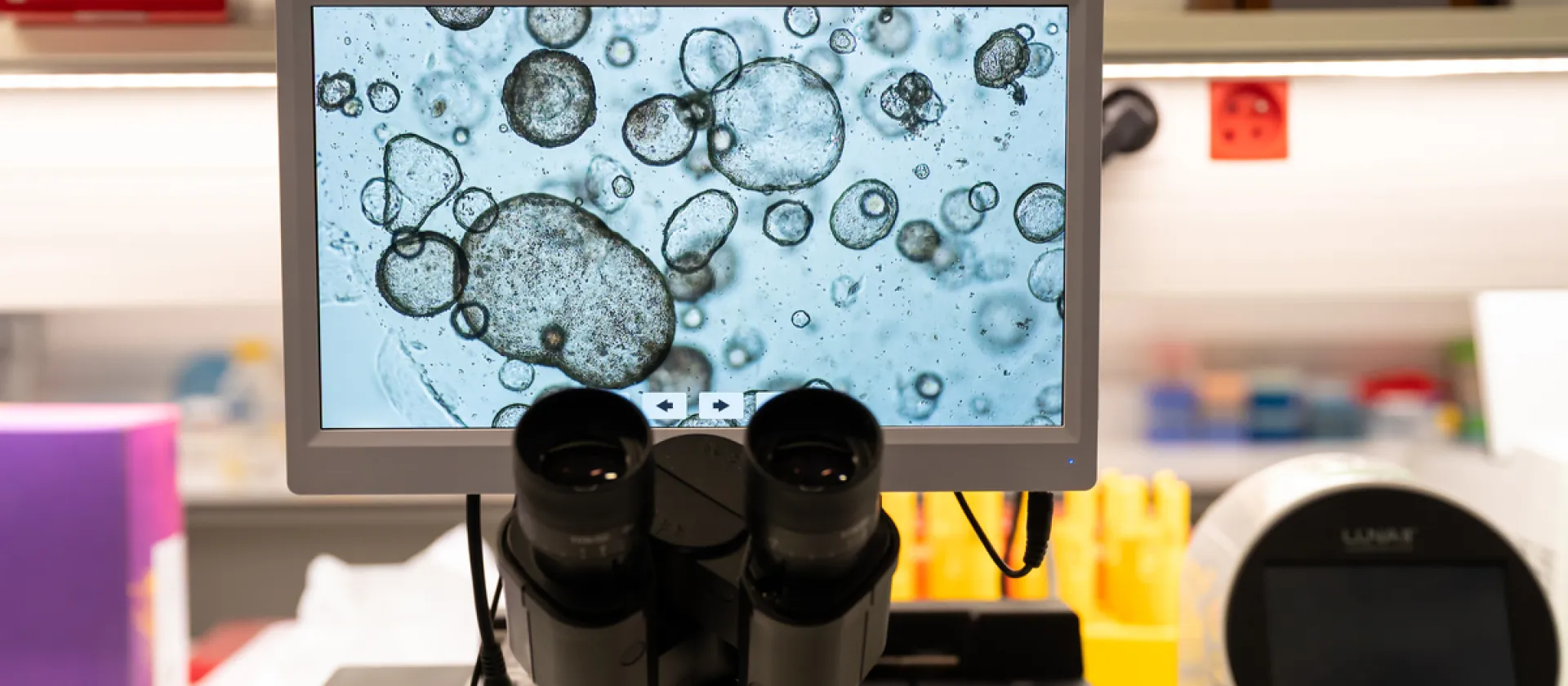
La Fondation Bettencourt Schueller soutient et encourage les chercheurs qui contribuent au rayonnement de notre pays dans les sciences de la vie. Cet engagement est le premier de la Fondation depuis sa création en 1987. S’il est principalement orienté vers la recherche fondamentale, sa finalité est l’amélioration de la santé humaine.
Soutien des chercheurs
Après un temps de réflexion stratégique, la Fondation Bettencourt Schueller a souhaité renforcer son engagement au côté des chercheurs et accélérer ses efforts pour conforter les atouts de la recherche française face aux grands défis qui se posent à notre société et contribuer à faire en sorte que la France demeure un grand pays de recherche. Depuis 2022, la Fondation déploie un programme de soutien des grands talents de la recherche en sciences de la vie en France : Impulscience. Destiné aux chercheurs en milieu de carrière, ce programme répond à deux impératifs : préserver la liberté d’innovation des chercheurs en France et les soutenir dans la durée.
Jusqu'à ce recentrage récent sur les chercheurs en milieu de carrière, la Fondation soutenait aussi des chercheurs par des dons directs. Ces dons étant pluriannuels, certains sont encore actifs aujourd'hui.
La Fondation décerne également deux prix annuels qui récompensent et encouragent les chercheurs à des moments clés de leur carrière : la création d’une équipe autonome avec la dotation du programme ATIP-Avenir, et la reconnaissance de découvertes exceptionnelles avec le Prix Liliane Bettencourt pour les sciences du vivant.
L’ensemble de ces soutiens dessine une filière d'excellence biomédicale dans la recherche française.
La Fondation développe également un ambitieux réseau d’animation et d’accompagnement des chercheurs soutenus, afin de favoriser de nouvelles collaborations et de nouvelles initiatives et collaborations.
Voir tous les lauréats des prix scientifiques
Voir tous les projets scientifiques soutenus
L'activité de mécénat en 2025
Pour qui agissons-nous ?
Le conseil scientifique
Les lauréats d'Impulscience et des prix scientifiques de la Fondation sont choisis par son conseil scientifique, à l’issue d’un rigoureux travail de sélection. Si chaque prix a son règlement, les grandes lignes en sont les suivantes : phase de candidature, examen de recevabilité et présélection des candidats par le conseil scientifique, expertises par des rapporteurs internes et externes, auditions et sélection par le conseil scientifique.
Le conseil scientifique de la Fondation est composé de quatorze personnalités scientifiques étrangères et françaises de premier plan. Assisté par l'équipe permanente de la Fondation, éclairé par des experts de renommée mondiale, il est entièrement indépendant et décisionnaire.
Composition
-

Professeur Hugues de Thé, président
Professeur au Collège de France, titulaire de la chaire Oncologie cellulaire et moléculaire – Paris. Membre de l'Académie des sciences – Paris.
-

Professeur Cédric Blanpain
Professeur de biologie du développement et cellules souches. Directeur de laboratoire des cellules souches et du cancer, Université libre de Bruxelles, Belgique. Membre de l'Académie royale de médecine – Belgique.
-

Docteure Deborah Bourc’his
Directrice de recherche à l’Inserm. Directrice de l’équipe « Décisions épigénétiques et reproduction » à l’Institut Curie – Paris.
-

Professeure Paola Bovolenta
Professeure Centro de Biología Molecular Severo Ochoa, Consejo Superior de Investigaciones Científicas, Universidad autónoma de Madrid – Espagne. Chaire du programme Tissue and Organ Homeostasis, Centro de Biología Molecular Severo Ochoa, CSIC-UAM.
-

Docteure Rosa Cossart
Directrice de recherche au CNRS. Directrice de l’équipe Empreinte du développement sur l’hippocampe adulte à l’Institut de neurobiologie de la Méditerranée (Inmed) – Marseille. Directrice de l’Inmed – Marseille.
-

Professeur Veit Hornung
Professeur d’immunobiochimie, Centre génétique et Département de Biochimie, Université Louis-et-Maximilien de Munich – Allemagne.
-

Professeur Xavier Jeunemaitre
Professeur des Universités de génétique et Praticien Hospitalier (PU-PH), Service de génétique à l’Hôpital Européen Georges Pompidou (HEGP) – Paris.
-

Professeur Gérard Karsenty
Professeur de génétique et développement, Columbia University – New York, Etats-Unis. Directeur du Département de Génétique et Développement, College of Physicians and Surgeons, Columbia University Medical Center – New York, Etats-Unis.
-

Professeur Marc Lecuit
Professeur des Universités, Praticien Hospitalier, Directeur de l'Unité de BIologie des Infections, Institut Pasteur, Inserm, Université Paris Cité, adjoint au chef du service de maladies infectieuses et tropicales de l’hôpital Necker-enfants malades.
-

Professeur Daniel Louvard
Directeur Honoraire, Institut Curie – Paris. Directeur de recherche émérite au CNRS – Paris. Professeur honoraire, Institut Pasteur – Paris. Membre de l'Académie des sciences. Membre étranger de l’American Academy of Arts and Sciences – Etats-Unis.
-

Docteur Marcel Méchali
Directeur de recherche classe exceptionnelle émérite au CNRS. Directeur de l’équipe Réplication et Dynamique du Génome, Institut de Génétique Humaine – Montpellier. Membre de l'Académie des Sciences, de l'Academia Europaea et de l'EMBO.
-

Professeure Miriam Merad
Professeure de cancérologie et d’immunologie. Directrice du Precision Immunology Institute et du Human Immune Monitoring Center, Mount Sinai School of Medicine – New York, Etats-Unis.
-

Professeure Molly Przeworski
Professeure de génétique des populations, Department of Biological Sciences, Columbia University – New York, Etats-Unis.
-

Professeure Gisou van der Goot
Professeure à la Faculté des Sciences de la Vie. Vice-présidente pour la transformation responsable à l’École Polytechnique Fédérale de Lausanne (EPFL) – Lausanne, Suisse.
Impulscience
Prix Liliane Bettencourt pour les sciences du vivant
Le Prix Liliane Bettencourt pour les sciences du vivant récompense chaque année un chercheur de moins de 45 ans pour l’excellence de ses travaux et sa contribution remarquable à son domaine de recherche scientifique.
Dotation du programme ATIP-Avenir
Le programme ATIP-Avenir favorise le retour ou l’installation en France de jeunes chercheurs de très haut niveau, porteurs d’un projet de recherche de qualité exceptionnelle, et désireux de créer leur propre équipe.